溶菌酶是一种天然的抗菌蛋白,具有优异的抗菌性能,可作为抗生素和化学防腐剂的替代品,解决细菌耐药性和食品安全问题。
溶菌酶存在于人体分泌液中,如唾液、眼泪、鼻涕,以及线粒体和蛋清中。
溶菌酶是免疫系统的一部分,能够杀灭革兰氏阳性菌。它通过与细菌表面结合,减少细菌的负电荷,并协助吞噬作用。缺乏溶菌酶会导致新生儿肺支气管发育不良和婴儿腹泻。眼泪中缺乏溶菌酶可能引发结膜炎。
某些癌细胞会分泌过量的溶菌酶,导致血液中溶菌酶含量过高,进而引发肾衰竭和低血钾。
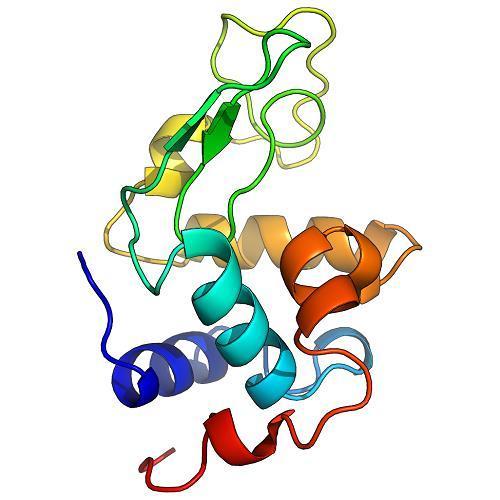
溶菌酶通过水解肽聚糖的糖苷键来攻击细菌细胞壁。它首先通过与肽聚糖分子结合,形成过渡态的构象。根据Phillips机制,溶菌酶与葡聚六糖结合,并将第四个糖扭曲为半椅形构象。在这种扭曲状态下,糖苷键容易断裂。
溶菌酶蛋白序列中的谷氨酸(Glu35)和天冬氨酸(Asp52)对其活性至关重要。Glu35作为糖苷键的质子供体,剪切底物的C-O键;而Asp52作为亲核试剂参与生成糖基酶中间体。随后,糖基酶中间体与水分子反应,水解生成产物,而酶保持不变。
溶菌酶广泛应用于实验室中对细菌的细胞破碎。
由于溶菌酶易于结晶,常被用于各种晶体学相关的研究。

