研究8-喹啉甲酸的合成途径和具体应用,有助于深入了解这一化合物的性质及其在相关领域的潜在价值。
背景:8-喹啉甲酸是一种重要的中间体,主要用作医药中间体、有机合成中间体等方面。目前国内外文献报道的主要合成路线是用8-甲基喹啉氧化得到8-喹啉甲酸,但8-甲基喹啉价格很高,没有大量生产,而且收率很低,只有35%;另外,还有文献用8-溴喹啉在低温条件下用丁基锂先做成 8-喹啉甲醛,再氧化生成 8-喹啉甲酸,此法用到的 8-溴喹啉市场只有克级提供,而且价格昂贵,方法也是需要用到低温和丁基锂,工业化困难。还有文献报道用邻氨基苯甲酸和甘油反应生成8-喹啉甲酸,此法是 Skraup 喹啉合成法,主要问题在于反应过程不易控制,反应会急速升温,小试时易冲料,放大反应会导致爆炸,无法实现工业化。
1. 合成:
(1)8-羟基喹啉三氟甲磺酸酯的制备
将8-羟基喹啉(275g,1.9mo1)溶于二氯甲烷(3L)中,加入三乙胺(249g,2.47mo1),降温至 0℃,然后滴加三氟甲磺酸酐(588g,2.1mo1)。反应在0℃反应1小时TLC跟踪反应完全,停止反应。500mL水加入反应釜中,搅拌 10分钟,分出二氯甲烷层,再用 500mL水洗,二氯甲烷层用无水硫酸钠干燥,蒸去二氯甲烷,得到粗品,用石油醚重结晶,得到白色固体 8-羟基喹啉三氟甲磺酸酯499g,收率95%。
(2)8-喹啉甲酸甲酯的制备
将 8-羟基喹啉三氟甲磺酸酯(300g,1.08mol)溶于甲醇(3L)中,然后加入催化剂双三苯基膦二氯化钯 15g,通入一氧化碳,加热至 110℃,0.8MPa,反应 12小时,反应完全后,降温,过滤掉催化剂,反应液蒸干得到油状物用 1L,乙酸乙酯溶解,用500mL水洗涤两次。无水硫酸钠干燥,过滤掉硫酸钠,蒸干溶剂,得到8-喹啉甲酸甲酯184g,收率 90.8%。
(3)8-喹啉甲酸乙酯的制备
将8-羟基喹啉三氟甲磺酸酯(300g,1.08mo1)溶于乙醇(3L)中,然后加入催化剂双三苯基膦二氯化钯 50g,通入一氧化碳,加热至 110℃,0.8MPa,反应 12 小时,反应完全后,降温,过滤掉催化剂,反应液蒸干得到油状物用 1L乙酸乙酯溶解,用500mL,水洗涤两次。无水硫酸钠干燥,过滤掉硫酸钠,蒸干溶剂,得到 8-喹啉甲酸乙酯195g,收率89.55%。。
(4)8-喹啉甲酸的制备
将 8-喹啉甲酸乙酯(150g,0.8mo1)溶于500mL乙醇中,加入25%氢氧化钠溶液(400mL),室温搅拌5小时,TLC显示反应完全。蒸去乙醇,降温,用称盐酸调 pH值到 5。得到大量固体,过滤,水洗,烘干,得到8-喹啉甲酸127g,收率98.4%。
2. 应用:合成2-喹啉基苯并咪唑衍生物。
苯并咪唑类化合物因其结构的多样性,良好的生物反应活性和光学性能等而被广泛地应用于化学化工、生命科学、材料、纺织和农业等领域,被用作催化剂、金属表面处理剂、分子探针、发光材料、助剂和农药等。因此,几十年来苯并咪唑及其衍生物的合成及应用的研究从未间断,新的化合物、新的用途不断地被报道。
李慧红等人在微波辐射下,通过8-喹啉甲酸和邻苯二胺(OPD)的酰胺化和脱水环化反应合成了3种新型的2-喹啉基苯并咪唑衍生物。具体实验步骤如下:
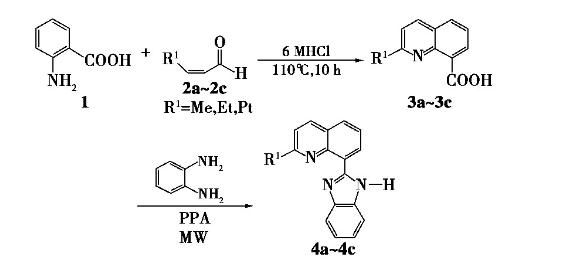
(1)中间体2-取代-8-喹啉甲酸(3a~3c)的合成
以2-甲基-8-喹啉甲酸(3a)的合成为例:取邻氨基苯甲酸13.71 g(100 mmol),6 mol/L的HCl 240 mL,依次加入到500 mL的三口烧瓶中,缓慢滴加2-丁烯醛12 mL(145 mmol),110℃回流反应 10 h。反应液冷却至室温,用氨水调pH至5,然后用二氯甲烷萃取反应液得到初产物。通过柱层析纯化,得白色固体14.11 g,产率是75.39%。
(2)2-喹啉基苯并咪唑(4a~4c)的合成
以2-(2-甲基-喹啉-8)-苯并咪唑(4a)的合成为例:将2-甲基-8-喹啉甲酸3.74 g(20 mmol)与1.5 eq的邻苯二胺及10.0 g(30 mmol)的PPA混合均匀,然后将混合物置于微波炉中,依次在解冻、中火、中高火3种模式下分别反应2、3 min和3 min,得深绿色溶液。反应液冷却至80℃,倒入冰水中,加KOH将其中和至pH=10~11,析出沉淀。抽滤,将滤饼分散至水中,用CH2Cl2萃取,得到粗产品。然后用柱层析除去杂质,旋干,所得产品用V(乙酸乙酯)∶V(水)=1∶1的混合溶剂重结晶,得产物4a 3.76 g。用同样的方法法制备4b和4c。
参考文献:
[1]李慧红,黄丹.微波辐射下2-喹啉基苯并咪唑衍生物的合成及表征[J].现代化工,2012,32(01):30-32+34.DOI:10.16606/j.cnki.issn0253-4320.2012.01.012.
[2]杰达维(上海)医药科技发展有限公司. 8-喹啉甲酸酯及8-喹啉甲酸的制备方法. 2011-10-19.

