2,4,5?三氟苯甲醛是一种重要的合成中间体,其合成与应用在医药领域具有广泛的研究价值。本文旨在探讨2,4,5?三氟苯甲醛的有效合成方法以及其在医药领域中的应用。
背景:2,4,5-三氟苯甲醛是一种重要的医药中间体,其可以制备2,4,5-三氟溴苄,2,4,5-三氟溴苄是日本盐野义药物Ensitrelvir(S-217622)的关键中间体,也是治疗糖尿病药物西他列汀的重要中间体。目前文献报道的2,4,5-三氟苯甲醛合成方法有以下几种:
1.以2,4,5-三氟甲苯为起始原料,与氯气进行侧链氯化生成2,4,5-三氟二氯苄,再水解生成2,4,5-三氟苯甲醛。此方法原料2,4,5-三氟甲苯价格高,不易得。
2.以2,4,5-三氟苯为起始原料,与一氧化碳/氯化氢混合气体在高压及lewis酸催化条件下发生Gattermann?Koch反应生成2,4,5-三氟苯甲醛。该方法同样存在着原料价格高,不宜得的缺点。
3.以2,4,5-三氟溴苯为起始原料,低温下与正丁基锂反应,后加入DMF生成2,4,5-三氟苯甲醛。该方法原料同样价格高,且反应条件苛刻。
合成优化:
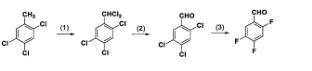
(1)惰性有机溶剂中,在蓝光照射下,将2,4,5-三氯甲苯与氯气进行如下所示的侧链光氯化反应,制备得到2,4,5-三氯二氯苄;(2)有机溶剂中,在氯化锌的存在下,2,4,5-三氯二氯苄进行如下所示的水解反应,制备得到2,4,5-三氯苯甲醛;(3)砜类溶剂中,在相转移催化剂的存在下,将2,4,5-三氯苯甲醛与氟代试剂进行如下所示的氟代反应,制备得到2,4,5-三氟苯甲醛。砜类溶剂为环丁砜和/或二甲基亚砜;相转移催化剂为四甲基氟化铵和/或四丁基氟化铵;氟代试剂为氟化钾和/或氟化铯。该制备方法收率高,总成本低,有经济价格优势。
应用:合成西他列汀。
1. 刘小卒等人以2,4,5-三氟苯甲醛为起始原料,与现场(in suit)生成的膦叶立德进行Wittig反应,给出相应的烯醇醚(Ⅱ),烯醇醚(Ⅱ)与(R)-叔丁基亚磺酰胺在无水ZnI2的作用下缩合得到手性磺酰亚胺(Ⅲ)。手性磺酰亚胺(Ⅲ)再经过 Mannich反应和酰胺化就可以实现西他列汀的不对称合成。其中2,4,5-三氟苯甲醛涉及的合成有:
(1)1,2,4-三氟-5-(2-甲氧乙烯基)苯(Ⅱ)的合成
于干燥的THF(600 m L)中加入(甲氧基甲基)三苯基氯化膦 (68.4 g,0.2 mol),冷却至0 ℃,充分搅拌下分批次加入叔丁醇钾 (22.4 g,0.2 mol),加完后升温至室温搅拌3小时,加入2,4,5-三氟苯甲醛(16 g,0.1 mol)后继续搅拌20小时。反应结束后冷却至 0 ℃,加入饱和氯化铵溶液(250 mL),减压浓缩除去有机相,剩余水相用乙酸乙酯(150 m L×3)萃取,无水硫酸钠干燥后,过滤,滤液浓缩后加入石油醚和乙酸乙酯混合液(v/v=10/1,400 mL),室温下搅拌30分钟,过滤,滤液浓缩,硅胶色谱柱纯化(PE/EA=20/1) 得淡黄色油状物(Ⅱ)(14.3 g,产率76 %)。
(2)(R)-叔丁基亚磺酰亚胺(Ⅲ)的合成
将第二步产物(Ⅱ)(9.4 g,0.05 mol)溶解于二氯甲烷(300 m L) 中,加入(R)-叔丁基亚磺酰胺(6.1 g,0.05 mol)和无水氯化锌(8.2 g, 0.06 mol),室温下搅拌12小时,过滤,减压浓缩得棕色油状物 (Ⅲ)(10.0 g,产率72 %)。
2. 张海军等人以2,4,5-三氟苯甲醛为起始原料,经Wittig反应,盐酸水解得到2-(2,4,5-三氟苯基)乙醛,再与(R)-(+)-叔丁基亚磺酰胺缩合得到对应的缩醛,得到的产物通过和溴乙酸乙酯的Reformatsky反应,然后水解得到对应的有机酸,该酸再和3-(三氟甲基)-5,6,7,8-四氢-[1,2,4]三唑并[4,3-a]吡嗪盐酸盐缩合得到西他列汀的叔丁基亚磺酰胺的缩醛,最后用盐酸甲醇脱保护得到西他列汀。该方法各步骤收率都较高,操作简单,所用试剂均为常规试剂,避免了使用昂贵的手性催化剂,有较好的工业化前景。
参考文献:
[1]刘小卒,韦文陶. 西他列汀中间体2-甲基-N-(2-(2,4,5-三氟苯乙酸)亚乙基)丙烷-2-亚磺酰胺的合成[J]. 广东化工,2018,45(16):42-43. DOI:10.3969/j.issn.1007-1865.2018.16.021.
[2]金雪芮. 基于纳米胶囊修饰的酶促反应体系构建与应用研究[D]. 天津:天津大学,2022.
[3]浙江巍华新材料股份有限公司. 一种2,4,5-三氟苯甲醛的制备方法:CN202211602597.8[P]. 2023-05-30.
[4]无锡佰翱得生物科学有限公司. 一种西他列汀的合成方法:CN201310320427.5[P]. 2014-01-01.

