引言:
合成Vindoline是一项具有挑战性和重要意义的化学研究课题,其合成方法和技术一直备受关注。通过不断的实验和探索,科学家们逐渐揭示了Vindoline的合成途径,为其工业化生产和药物研发提供了重要的参考和指导。
1. Vindoline 合成简介
长春碱 和长春新碱是一类双吲哚生物碱中最广泛认可的成员,因为它们在临床上用作抗肿瘤药物。至今长春碱和长春新碱仍主要从长春花植物中提取,长春花是该生物碱的唯一来源植物。由于这两种生物碱在植物体内含量很低,分别为十万分之几和百万分之几,并无法用化学合成的方法生产,使市场价格非常高。尽管其在临床上有剂量依赖的神经毒副作用,使其应用受到一定限制。但由于其广泛的临床和其它应用及改造潜力,药物化学家们仍在努力试图用化学方法合成它们,或进行结构改造以寻求高效低毒的类似物。生物学家也很早便开始研究用植物组织细胞培养的方法来生产这些生物碱。
自60年代国外就开始研究长春花组织培养生产吲哚生物碱,从70年代末开始,用此来生产长春花生物碱的研究成为生物工程领域的一个热点,但至目前为止,仍未能从悬浮培养细胞中获得这两种抗癌生物碱,仅可生产阿玛碱、蛇根碱和长春质碱,也未能实现工业化生产。由于文多灵是目前半合成长春碱或长春新碱的重要前体物质,也就是说可以用长春质碱和文多灵在体外人工半合成长春碱。所以只要用植物细胞大规模培养生产出长春质碱和文多灵这两种原料,就可以半合成长春碱。Vindoline的结构如下图所示:
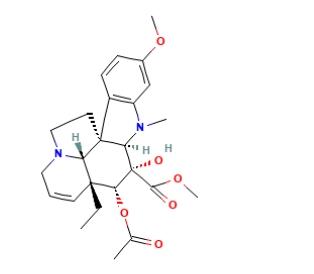
2. Vindoline 合成方法
可以通过两种主要方法合成:A. 全化学合成:该方法完全在实验室中从现成的起始材料构建vindoline;B. 生物合成:该方法利用基因工程微生物从较简单的前体生产vindoline。以下是每种方法的细分:
2.1 全化学合成
(1)环加成反应
这些反应通过连接两个分子形成新的环。Boger合成是一个著名的例子,它利用串联[4+2]/[3+2]环加成级联在vindoline的核心结构中同时产生三个环。
(2)立体选择反应
Vindoline有多个立体中心(具有特定空间排列的原子)。化学家在合成过程中采用各种技术来确保这些中心的正确三维排列。对映选择性催化和手性起始材料是用于此目的的一些策略。
(3)官能团操纵
在整个合成过程中,化学家引入各种官能团(如羰基、醚),并通过还原、消除、保护/去保护等反应对其进行有策略的操纵,以获得最终的vindoline结构。
2.2 生物合成:
(1)代谢工程
科学家将Catharanthus roseus(马达加斯加长春花)的vindoline生物合成途径的基因引入酵母。这使酵母具有将较简单的前体如他伯松碱转化为vindoline的酶能力。
与复杂的化学合成相比,生物合成为vindoline生产提供了一种潜在的更可持续和可扩展的方法。
3. Vindoline 的酶法合成
3.1 vindoline合成的酶促途径解释
Vindoline生物合成是在马达加斯加长春花(Catharanthus roseus)中发现的一个复杂的自然过程。它涉及从萜类中间体焦磷酸香叶基开始的多个酶促步骤。主要酶包括:
香叶醇合成酶(GES)
香叶醇8-羟化酶
8-羟基香叶醇氧化还原酶(GOR)
环烯醚萜合成酶
Tabersonine 3-加氧酶
Tabersonine 3-还原酶
3-hydroxy-16-methoxy-2 3-dihydrotabersonine-N-methyltransferase (NMT)
Desacetoxyvindoline-4-hydroxylase (D4H)
Deacetylvindoline-4-O-acetyltransferase (DAT)
这些酶共同作用,通过一系列羟基化、氧化、环化、甲基化和乙酰化反应,依次将香叶基焦磷酸转化为vindoline。
3.2 生物催化剂及其在这一过程中的作用:
在这种情况下,生物催化剂是指上面提到的酶。每种酶都像催化剂一样,是一种特殊的蛋白质,可以加速特定的化学反应而不被自身消耗。它们在vindoline合成中起着至关重要的作用:
(1)选择性
酶是高度选择性的,这意味着它们只针对特定的底物并促进所需的反应。这最大限度地减少了不必要的副反应,并允许vindoline的有效形成。与传统的化学合成相比,酶可以在温和的条件下(温度、压力、pH值)工作。这减少了能源消耗,使过程更加环保。
(2)立体控制
许多酶可以控制产物分子的立体化学。Vindoline具有具有多个手性中心的特定3D结构。酶确保这些中心的正确排列,对最终产品的生物活性至关重要。
4. 具体合成实例
4.1 方法一
Danieli等人开发了一种将更丰富的tabersonine转化为11-甲氧基tabersonine,然后转化为vindoline的方法。由于无法清洁有效地实现对tabersonine和2,16-二氢-drotabersonine的亲电取代,因此选择N-乙酰基-2,16-二氢tabersonine作为底物。硝化反应得到10-硝基衍生物的高产率,然后通过标准工艺将其转化为11-甲氧基-2,16-二氢塔伯森碱(379),该衍生物作为C-16差向异构体的混合物获得。尝试用苯亚硒酸酐脱氢到11-甲氧基塔伯森碱偶然伴随着所需的C-17 β-羟基的引入。将产物380通过前面描述的合成长春多氨酸的方法转化为Vindoline。
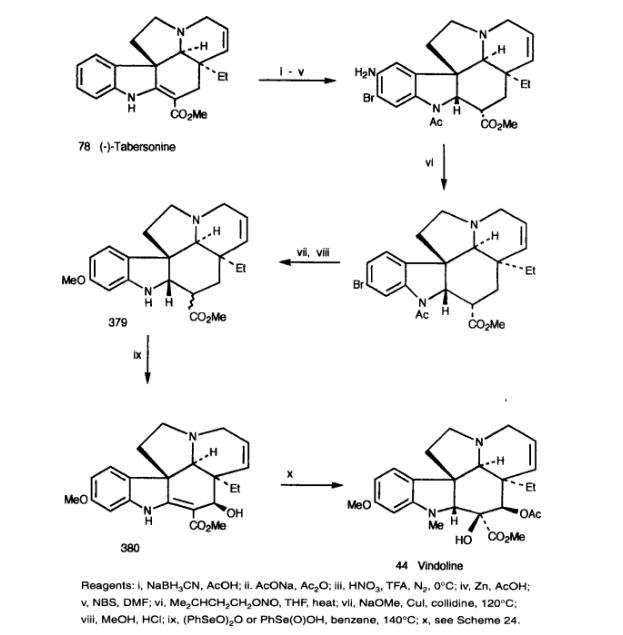
4.2 方法二
4.2.1 长春花细胞系的培养
(1)长春花愈伤组织的获得
将长春花的幼茎作为外植体,用70%的乙醇表面杀菌30-50秒后投放到5-15%次氯酸钠溶液中二次杀菌10-20分钟,然后用无菌水冲洗三次,取出后在超净工作台中将幼茎切成2毫米长的茎断,接种到脱分化培养基中,在2000lx,12-16小时照光,25度左右室温下培养3-4周,即可获得白色愈伤组织。再将愈伤组织放在步骤2)所述继代驯化培养基中继代培养3次以上,同时筛选得到生长速度快,质地松软,生长量稳定的细胞系。
(2)脱分化培养基的配制
在MS培养基中,添加吲哚乙酸1.0mg/L,细胞分裂素6-BA1.0mg/L,20g/L蔗糖,然后用酸或碱将pH值调整到5.8,再添加6.5g/L琼脂,在115℃,0.1MPa压力下消毒15分钟后,经冷却制成斜面脱分化培养基。
(3)长春花愈伤组织块的继代驯化培养
将以上步骤诱导形成的愈伤组织细胞系接种在下述继代培养基中进行3次以上的继代培养,培养条件为20℃室温,避光条件,培养周期为3周。在继代培养过程中,筛选出结构疏松以及生长速度较快的愈伤组织进行继代培养;
继代驯化培养基的配制:在MS培养基的基础上添加1.0mg/L的植物细胞生长素NAA,1.0mg/L的植物细胞分裂素6-BA,20g/L蔗糖、6.5g/L琼脂,经115℃,0.1MPa压力下消毒15分钟后经冷却制成平板继代驯化培养基。
(4)长春花多倍体细胞的诱导
在MS培养基中加入10mg/L秋水仙碱(Sigma,C3915),做成液体诱导培养基,将获得的结构疏松生长速度较快的愈伤组织接种在该诱导培养基内,在20℃,避光,100rpm/分转速的摇床上振荡培养7天。收集细胞后再接种在无秋水仙碱的继代培养基中,反复驯化培养三次以上,通过生物积累量测定筛选到生长速度更快(生长速度超过5倍接种细胞量/培养周期)的多倍体细胞系;经细胞醋酸洋红或银染色后通过显微检测表明,该细胞系为混合多倍体细胞系。
(5)长春花多倍体细胞的扩增培养
将得到的长春花混合多倍体细胞系接种在扩增培养基上,在25℃,黑暗条件下进行扩增培养3周后,获得接种量10倍以上的生长旺盛的多倍体细胞;
扩增培养基的制备方法为:在改良MS培养基(按照Murashige&Skoog培养基的配方,将其中的CuSO4·5H2O和CoCl2·6H2O的添加量提高到0.1mg/L,再添加1mg/L的抗坏血酸得到的培养基)中,添加2mg/Lα-萘乙酸(NAA),2mg/L6-卞氨基嘌呤(6-BA)和30g/L蔗糖,然后用酸或碱将pH值调整到5.7,再添加4.5g/L琼脂,在115℃,0.1MPa压力下灭菌15分钟后,制成扩增固体培养基。
4.2.2 文多灵合成
将扩增培养得到的生长旺盛长春花多倍体细胞接种到合成培养基内,接种量为200g/L,在25℃,避光条件,90转/分的摇床或大型生物反应器中悬浮培养7天得到富含文多灵的细胞。收获细胞,培养液经调整后可返回反应器继续反复利用。
合成培养基:在改良MS培养基(按照Murashige&Skoog培养基的配方,将其中的CuSO4·5H2O和CoCl2·6H2O的添加量提高到0.1mg/L,再添加1mg/L的抗坏血酸得到的培养基)中,添加蔗糖30g/L,吲哚乙酸(IAA)1mg/L,KT 1mg/L,用酸或碱将pH值调整到5.8,在115℃,0.1MPa压力下消毒15分钟后冷却处理;冷却后再添加过滤除菌的组合前体(乙酰辅酶A 10μg/L、苯丙三氮唑0.5μmol/L、苯环丙胺5μmol/L、乙酸酐10μl/L、二硫苏糖醇10mg/L),用无菌的酸或碱将pH值调整到5.8,制成合成培养基;
4.2.3 文多灵的提取
将合成培养得到的富含文多灵的细胞置于提取灌中,经过高速搅拌(300转/分)破碎,加入1ml/g鲜细胞量的体积百分浓度为95%的乙醇溶液,在室温条件下萃取,然后减压(0.01MP)浓缩获得粗提物,再加入二倍体积的乙酸乙酯,用硫酸调pH值为8.0后,迅速摇荡,萃取生物碱三次,减压蒸干后获得含有文多灵的混合物。用高效液相色谱(HPLC)检测该混合物中文多灵的含量,结果表明,文多灵含量达到1mg/g细胞干重。
5. 合成 Vindoline 的应用和用途
(1)合成Vindoline的各种应用综述
合成Vindoline的主要应用在于它作为重要抗癌药物长春碱和长春新碱的前体。长春花属植物中长春花碱的天然丰度很低,化学合成也很困难,这使得合成Vindoline成为大规模生产这些救命药物的有价值的替代品。
(2)在制药和其他行业的潜在用途
除了它作为前体的既定作用之外,人们正在研究合成vindoline本身的潜在应用:
抗糖尿病特性:研究表明,vindoline可能具有抗糖尿病作用,尽管需要更多的研究来证实其作为一种治疗方法的有效性。
新药开发:合成vindoline独特的化学结构为开发具有多种治疗应用的新型药物提供了希望。通过修改vindoline分子,科学家们有可能制造出针对各种疾病的药物。
6. 结论
总的来说,合成Vindoline是一项具有挑战性和前瞻性的研究领域,其合成方法的不断完善和优化将为药物研发和生产提供重要的技术支持和指导。希望本文对Vindoline的合成方法有所启发,激发读者对这一领域的兴趣和探索。
参考:
[1]https://pubchem.ncbi.nlm.nih.gov/compound/260535
[2]https://www.sciencedirect.com/topics/chemistry/vindoline
[3]https://www.nature.com/articles/s42003-021-02617-w
[4]https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2531198/
[5]清华大学. 一种生产文多灵的方法. 2008-12-31.

