西蒙斯-史密斯反应 (Simmons-Smith reaction) 是以化学家 H. E. Simmons 及 R. D. Smith 命名,在 1958 年所提出,将不具有官能基的烯类化合物进行环丙烷化的反应,具有良好的立体专一性。此反应是先利用锌铜偶 (zinc-copper couple) 将二碘甲烷製成西蒙斯-史密斯类碳烯试剂(以下简称西-史试剂),接着再将西-史试剂与烯类化合物进行反应,最终可得到具有环丙烷基的产物。(图一)

图一、西蒙斯-史密斯反应示意图 (作者绘製)
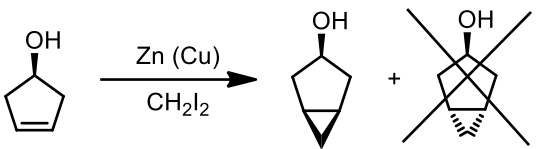
反应步骤如下,首先是锌铜偶的製备。锌铜偶其实是一种被铜所活化的锌,本质上是锌铜的合金,但并没有严格的结构及成分定义(一般而言锌的比例会大于锌铜偶的 图二、西蒙斯-史密斯试剂性质示意图(作者绘製) 一旦製得西-史试剂后,便可将其与含烯类官能基的化合物进行反应。而此反应的反应机构是一连续性的步骤:烯类的双键之 图三、西蒙斯-史密斯反应机构 (作者绘製) 西蒙斯-史密斯反应具有以下特性: (1) 良好的立体专一性;(2) 可进行环丙烷化的烯类种类广(简单烯类、共轭烯酮…...);(3) 由于西-史试剂要受到烯类的亲核加成,所以电子较为充裕的烯类 (electron rich) 其环丙烷化速率较快;(4) 考虑立体障碍,若是接有较大取代基之烯类反应速率较慢;(5) 较少副反应的产生,目前为有机合成上主要的环丙烷化方式。 最初的西蒙斯-史密斯反应只是以二碘甲烷将烯类进行环丙烷化,而到了 1966 年,古川教授 (Furukawa) 对于此反应的条件进行修改,其利用二乙基锌作为锌的来源,而溶剂也从乙醚改为不具配位能力的有机溶剂(如二氯甲烷、1, 2-二氯乙烷),而比较特别的一点在于可以利用具有取代基的碘烷与烯类进行环丙烷化。(图四) 图四、古川修正过的西蒙斯-史密斯反应 (作者绘製) 此外,西蒙斯-史密斯反应最广为人知能够控制其反应立体位向的因素就是化合物本身存在羟基的位向,西-史试剂对于烯类进行环丙烷化的位向总是与化合物本身羟基的方向相同。 考虑以下例子:如果将 3-环戊烯-1-醇进行西-史反应,则最终环丙烷基产生的方向与羟基的方向必在五员环的同一边(图五)。原因是羟基的氧的电子可能会配位至西-史试剂的锌上,使得西-史试剂只会和羟基在五员环的同一边与烯基进行环丙烷化反应,这也是西蒙斯-史密斯反应相当重要的特性。 图五、羟基诱导立体专一性的西蒙斯-史密斯反应 (作者绘製) 参考文献


http://www.organic-chemistry.org/namedreactions/simmons-smith-reaction.shtm

