本文旨在介绍制备十二水硫酸铝铵的方法,通过详细步骤和操作要点,帮助读者了解该化合物的制备过程。
简述:由于NH4Al(SO4)2·12H2O在水中结晶性及过滤性能好,在一定温度下焙烧后易转化成氧化铝等等特性已被广泛作为制备铝系产品中一种重要的中间产物。Hostomska等通过调节地下铀矿硫酸浸出液中的Al3+/NH+4,通过结晶络合生成十二水硫酸铝铵晶体,实现废液中Al3+及NH+4的回收利用;Lin等在处理了铝合金的酸废液中加入(NH4)2SO4得到十二水硫酸铝铵晶体,达到铝回收利用的目的。
十二水硫酸铝铵的制备:
1.方法一:
利用硫酸作浸取剂可形成含有Al2(SO4)3、Na2SO4、Fe2(SO4)3、K2SO4等硫酸混盐的浸取液。可以通过向含有Al2(SO4)3酸浸液中加入(NH4)2SO4络合反应生成在低温时易结晶析出的NH4Al(SO4)2·12H2O,从而实现铝的高效分离。粉煤灰提取氧化铝是粉煤灰高值化利用的重要方向。通过在粉煤灰酸浸液中加入硫酸铵形成常温下可结晶的十二水硫酸铝铵晶体(NH4Al(SO4)2·12H2O),从而实现铝盐的高效分离。具体步骤如下:
(1)酸浸液的制备
分别称取100g粉煤灰与80gNa2CO3(质量比1∶0.8)混合均匀至粉末状,至于850℃的马弗炉中煅烧2h;将煅烧得到的物料冷却至室温并用球磨机研磨30min后至于45℃的烘箱中2h;准确称取20g干燥后的物料与100mL25%的硫酸(液固比为5)混合后,至于250mL的四口烧瓶内,在98℃酸浸2h后进行抽滤,用15mL沸水对滤饼冲洗3次后,取酸浸液进行结晶实验。酸浸液主要含金属离子为Al3+、Na+、Fe3+、K+、Ca2+,对应含量分别为0.46、0.56、0.054、0.031和0.013mol/L。由于粉煤灰活化时需要加入助剂Na2CO3,所引入Na+成为杂质中浓度最高的离子。准确量取200mL含Al2(SO4)3的酸浸液,向酸浸液中添加一定量Al2(SO4)3,加热至50℃,确定Al2(SO4)3完全溶解,冷却至室温,得到含有不同Al3+浓度的酸浸液。
(2)十二水硫酸铝铵晶体的制备
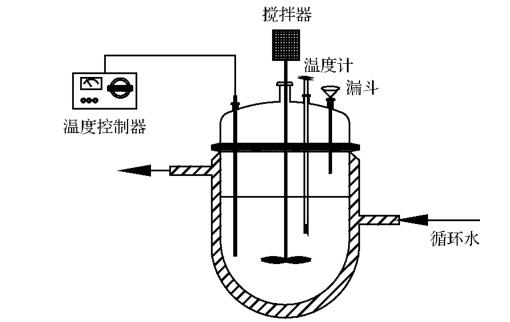
准确量取100mL含一定铝离子浓度的酸浸液,加入0.5L结晶反应器中(下图为结晶反应装置);设定一定的温度,开启搅拌器,转速为300r/min;将一定质量的(NH4)2SO4加入到酸浸液,恒温搅拌2h;反应结束后用真空泵对结晶液进行过滤,并用30mL无水乙醇清洗滤饼3次,最后将滤饼置于温度为45℃的鼓风干燥箱中2h后取出。
2. 方法二:
冷却结晶法制备NH4Al(SO4)2·12H2O,具体步骤如下:
称取 2.7gNHC1和 29.9g十八水合硫酸铝,放人100mL烧杯中,加50mLH20,用1mol/L稀硫酸调 pH至1.5,加热至90℃,待盐全部溶解后,继续加热1~2min,并不断搅拌。然后,快速将烧杯转移到水浴槽中(T=10℃~20℃),静置。冷却至25℃~30℃,即有大块结晶析出。
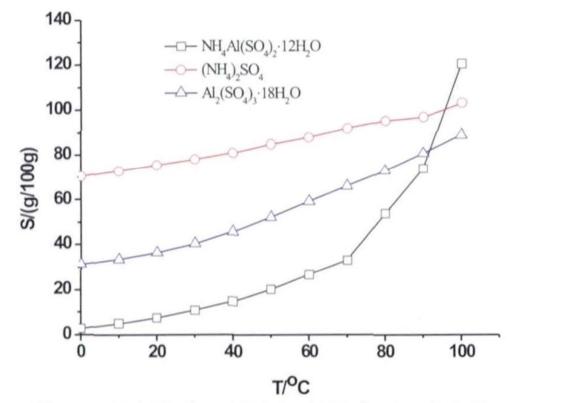
实验原理为:在含NH+4、Al3+、S02-4,等离子的溶液体系中,如果某些条件发生变化(比如温度等),则可能出现Al2(SO4)3·18H20、( NH4)2SO4、NH4Al(SO4)2·12H20等沉淀。其中,NH4Al(SO4)2·12H0受温度的影响最大(如下图所示),其溶解度随温度升高变化很大,从0℃~100℃,溶解度增大 40多倍而 Al2(SO4)3:·18H20和(NH4)2S04的溶解度随温度的升高变化不大。因此,控制反应在较高温度下进行,然后冷却使复盐NH4Al(SO4)2·12H20结晶析出,如方程式(1)所示。
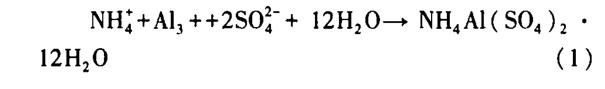
参考文献:
[1]赵瑜,谢宇琪,郭彦霞等. 利用粉煤灰硫酸浸取液制备十二水硫酸铝铵 [J]. 环境工程学报, 2015, 9 (12): 6034-6040.
[2]王崇臣,王鹏. 十二水硫酸铝铵的制备与表征 [J]. 实验室科学, 2013, 16 (06): 4-6.

