本文将介绍2-脱氧-L-核糖的合成方法,这对于理解该化合物的制备过程以及在化学合成等领域的应用具有重要意义。
背景:L-核苷及其类似物具有抗病毒活性和较低的毒性而受到越来越多的重视,目前,已有3个L-构型的核苷类药物上市:拉米夫定、恩曲他滨和替比夫定,并有多个L-核苷类,化合物正在进行临床研究,L-核苷类化合物已成为抗病毒药 物研究和开发的新热点。2-脱氧-L-核糖作为合成L-核苷类化合物的重要原料,它的合成研究受到广泛关注。
合成:
1. 方法一:以3-羟基-1,4-戊二烯为原料合成
Tung等以3-羟基-1,4-戊二烯(17)为起始原料,经Sharpless环氧化反应,以100%对映选择性得到端基环氧化的不饱和醇,羟基保护后,运用硼氢化/氧化将端基双键转化为羟基,再经Swern氧化得 到醛,环合后得到2-脱氧-L-核糖,总收率25%。
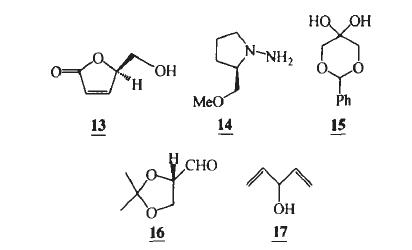
2. 方法二:α,β-不饱和内酯的非对映选择性加成合成法
α,β-不饱和内酯经1,4-加成后再将酯羰基还原为醇羟基,可得到2-脱氧核糖,但易得到外消旋体。Fazio等利用经济易得的(R)-(+)-5-羟甲基-5H-呋喃-2-酮 (8)与(PhMe2Si) 2Cu(CN)Li2 的1,4-加成反应达到完全非对应选择的效果。
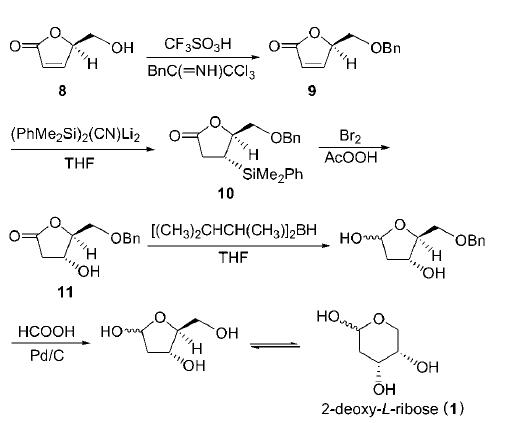
该反应以(R)-(+)-5-羟甲基-5H-呋喃-2-酮(8)为原料,5-羟甲基经苄基保护后与(PhMe2Si) 2Cu(CN)Li 2 发生 1,4-加成,高选择性地得到产物10,产物10用Br2在 AcOOH存在下全部转化为羟基衍生物11,且构型完全保持,11经氧化后再脱去苄基,得到2-脱氧-L-核糖(1)。由于苄基的引入促进了硅基铜酸盐试剂在迈克尔体系中的非对映选择性加成,使PhMe2Si全部进入反位,硅基官能团能完全构型保持地转化为羟基,使反应能高选择性地进行,避免了外消旋体的产生,解决了对映体难以分离的问题,有一定的应用价值。
3. 方法三:高立体选择性炔丙化作用
胡守刚等利用逆合成法,通过在保护的甘油醛 13端基借助锌的作用高立体选择性地引入炔丙基,再对端基不饱和键进行立体选择性地部分还原,臭氧化后在酸性条件下脱保护,合成了2-脱氧-L-核糖。
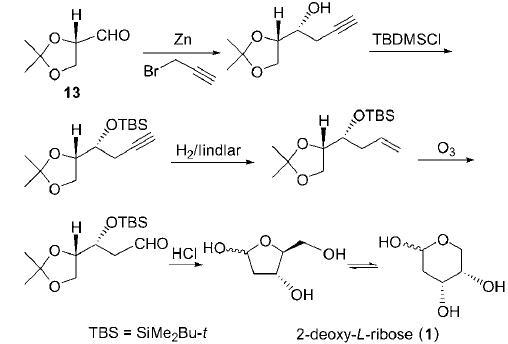
在该反应中,锌对炔丙基溴与2,3-氧-异亚丙基-L- 甘油醛(13)的非对应选择性反应起到了关键作用,而有机镁、金属铟等类似化合物的效果较差。该方法具有良好的立体选择性,在不使用辅助试剂的情况下,避免了繁杂的分离过程,是一种以增碳反应合成L-脱氧核糖的有效方法,也可用于D-脱氧核糖及其衍生物的合成。
4. 方法四:不对称烷基化作用
Ulven等用辅助剂RAMP [(R)-1-氨基-2-甲氧甲基吡咯烷]对被保护的2-苯基-1,3-二氧杂环己酮(12)进行烯丙基溴的不对称烷基化,生成占90%的4-位烯丙基取代物,加入NH4H 2PO 4 缓冲溶液,调节溶液pH>12. 去掉辅助剂后,用Na BH4还原,得羟基处于平伏键上的醇的含量上占绝对优势,臭氧化后得2-脱氧-L-核糖。
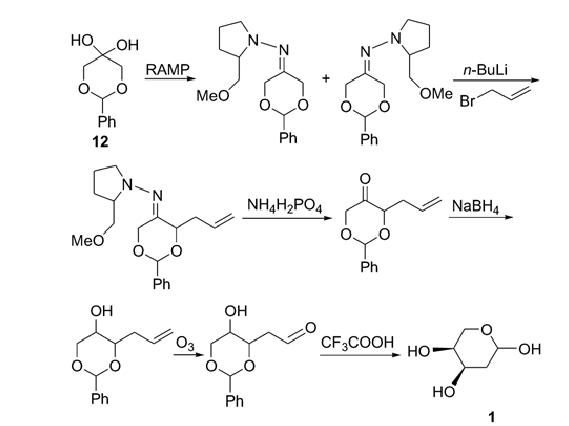
该路线借助于辅助剂RAMP生成的腙与被保护的小分子2-苯基-1,3-二氧杂环己酮(12)反应,达到不对称烷基化的目的,实现了较好的立体选择性,开辟了一条合成2-脱氧-L-核糖的新途径。
参考文献:
[1]汤军,吴建国. 2-脱氧-L-核糖重要中间体2-脱氧-α-1,3,4-O-苯甲酰-L-阿拉伯吡喃糖的合成工艺改进 [J]. 中南药学, 2009, 7 (01): 9-11.
[2]邓达,卓超,陈友. 2-脱氧-L-核糖的合成方法进展 [J]. 精细化工中间体, 2007, (02): 9-12. DOI:10.19342/j.cnki.issn.1009-9212.2007.02.003
[3]韩素辉,渠桂荣,李永. 2-脱氧-L-核糖的合成方法研究概况 [J]. 有机化学, 2005, (05): 526-531+479.

