通过探索柚皮素的制备方法以及其在溶解度、稳定性和生物活性等方面的理化性质,我们可以为其在药物开发和应用领域提供更有效的利用途径。
简介:虽然柚皮素具有广泛的药理活性,但由于其水溶性和脂溶性均不好,易氧化,体内吸收差,口服生物利用度较低等缺点,限制了其临床应用。据文献报道以游离柚皮素计,柚皮素在兔体内的生物利用度仅为4%。目前市面上还没有柚皮素相关产品,国内科研工作者尝试通过给柚皮素连接水溶性基团或制成固体分散体、包合物、自微乳等各种剂型来提高其生物利用度,以期早日开发出可上市的新产品。
1. 萃取法
直接从天然植物中萃取是提取柚皮素的一个主要方法。陈雪峰等采用传统的有机溶剂法提取桃叶中的柚皮素,通过试验确定了柚皮素的最佳提取条件为:乙醇、甲醇浓度比7∶3,温度为50℃,时间为5 h,料液比为1∶45 (g/ml),该条件下的柚皮素收率为5.25%。此外,陈雪峰等还采用超临界CO2技术从桃叶中提取柚皮素,其最佳提取工艺为:萃取温度60℃,压力30 MPa,时间6 h,料液比为1∶2 (桃叶与95%乙醇的质量比),该条件下柚皮素的收率达到 2.18%。采用绿色清洁的超临界CO2技术从价格低廉的桃叶中提取柚皮素,具有重要的经济价值。沈忠明等则采用溶剂萃取法从中药菝葜(百合科菝葜属植物)中提取柚皮素。
2. 柚皮苷水解法
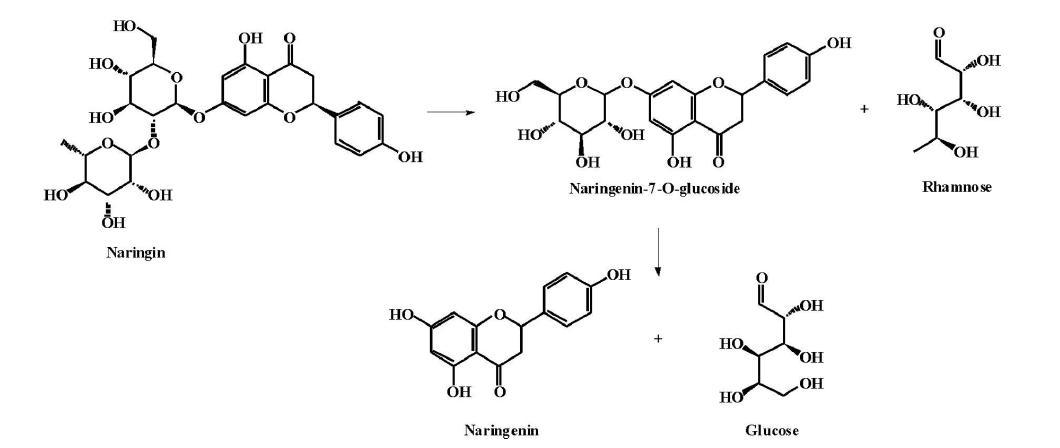
柚皮苷(Naringin,CAS 10236-47-2)也是一类天然黄酮类化合物,广泛存在于柚子、葡萄柚、酸橙及其变种的果实和果皮中。柚皮苷水解法是制备柚皮素的另一个主要方法,包括生物水解法和化学水解法。雷生姣等报道的一种由α-L-鼠李糖苷酶(α-L-rhamnosidase)和 β-D-葡萄糖苷酶(β-D-glucosidase)组成的混合柚苷酶,具有 α-L-鼠李糖酶和β-D-葡萄糖苷酶的活性,可以有效地水解柚皮苷,如图所示。水解柚皮苷主要分2步完成,首先,柚皮苷被鼠李糖苷酶水解为鼠李糖(Rhamnose)和柚皮素-7-O-葡萄糖苷 (Naringenin-7-O-glucoside),柚皮素-7-O-葡萄糖苷的苦味约为柚皮苷的1/3;然后,柚皮素-7-O-葡萄糖苷又在β-D-葡萄糖苷酶的作用下被水解为无苦味的柚皮素和葡萄糖(Glu cose)。郑美瑜等则进一步研究了柚苷酶对柚皮苷单体的酶解条件为:酶解液中底物质量浓度为25 g/ml,酶含量为1 U/ml,酶解时间为1.0~1.5 h。Kratky等则采用化学水解法,以三氟乙酸或盐酸为催化剂,把柚皮苷部分水解为鼠李糖和柚皮素-7-O-葡萄糖苷。
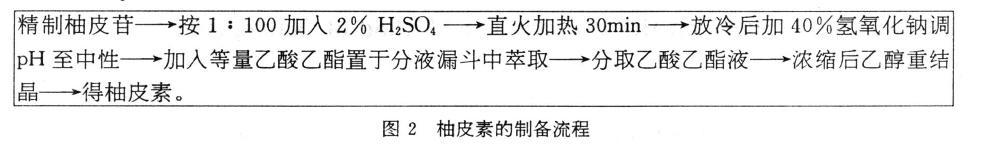
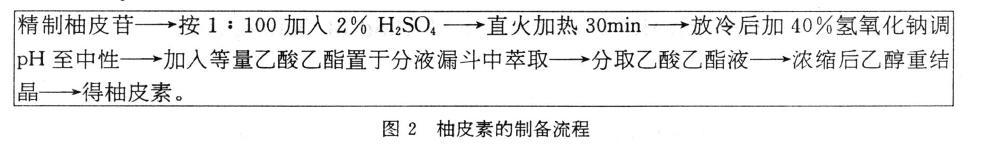
3.刘亚萍首先采用水作为溶剂从化橘红中提取柚皮苷,精制后的柚皮苷采用硫酸作为催化剂,完全水解得到柚皮素,经核磁共振鉴定所得柚皮素为高纯度的柚皮素。
3.1 柚皮苷的制备

3.2 柚皮素的制备
所得柚皮素呈白色,针晶(乙醇),mp:246—249℃ 。盐酸镁粉反应呈樱红色,四氢硼钠反应呈红紫色,molish反应阴性。分别以95%乙醇为展开剂,进行聚酰胺薄层层析、石油醚:乙酸乙酯(2∶1 )为展开剂进行硅胶薄层层析检查,三氯化铁显色,均显示单一斑点。
3.3 柚皮苷在酸碱条件下,二氢黄酮苷元易分解,所以选用水提取,效果更好。
由于柚皮素是二氢黄酮,在水中有一定溶解度,所以水解液中和后以乙酸乙酯萃取,去除未水解苷和糖,但所得苷元一定要用乙醇反复重结晶才能得到高纯度的柚皮素。
4. 理化性质研究
柚皮素(4',5,7-三羟基二氢黄酮)是柚皮苷水解掉一分子葡萄糖和鼠李糖得到的苷元。常温下为白色针状晶体,储存条件一般为阴凉干燥环境,分子式为C15H12O5,分子量为272.25, 熔点247~250℃,由于其分子内含有苯环、羟基、羰 基等官能团,所以在紫外区有吸收,无水乙醇中其紫外光谱在288 nm处有最大吸收。柚皮素溶于乙醇、乙醚和苯,几乎不溶于水。盐酸镁粉反应呈樱红色,四氢硼钠反应呈红紫色, molish反应阴性。脂溶性和水溶性不甚理想,通过引入脂溶性或水溶性较强的基团对其结构进行修饰,可提高其脂溶性或水溶性,从而提高生物利用度。其结构修饰主要包括羟基的烷基化、酰化、磺化、苷化及形成金属配合物等。
参考文献:
[1]季鹏,赵文明,于桐.柚皮素的最新研究进展[J].中国新药杂志,2015,24(12):1382-1386+1392.
[2]吕爱新,于宏伟,赵志强等.柚皮素研究进展[J].安徽农业科学,2011,39(13):7734-7735+7845.DOI:10.13989/j.cnki.0517-6611.2011.13.220.
[3]刘亚萍.柚皮素的制备方法研究[J].光谱实验室,2008(06):1292-1294.

