L-2-氨基丁酸是一种非天然手性氨基酸,可用作手性药物的前体,用于抑制神经信息传递和促进脑细胞代谢。它可以通过酰胺化制备抗癫痫药物左乙拉西坦和布瓦西坦的关键前体氨基丁酰胺,也可以通过还原L-2-氨基丁酸制备抗结核药物乙胺丁醇的关键手性中间体。
目前,传统的化学制备方法因成本高、能耗高、污染严重、光学纯度低等缺点失去了竞争力,因此生物制备成为研究的热点。最近的研究表明,利用L-苏氨酸为底物,通过苏氨酸脱氨酶、亮氨酸脱氢酶和甲酸脱氢酶的一锅法转化制备L-2-氨基丁酸,可以获得高达97.3%的收率。然而,该方法需要构建多种基因的生物催化剂,并且操作繁琐,增加了生产成本和工艺要求。因此,我们需要构建多酶级联催化的单细胞以实现高效的L-2-氨基丁酸生物制备。
本研究通过分子动力学模拟软件计算分析,发现截短亮氨酸脱氢酶的Loop区域可以显著提高酶活力。此外,通过双拷贝亮氨酸脱氢酶和甲酸脱氢酶的多酶催化平衡,构建了单细胞E. coli BL21/pACYCDuet-RM菌株。该菌株在最适条件下转化L-苏氨酸,产量达到最大值66.4 g/L,产率接近100%。
通过5 L发酵罐全细胞转化制备,可以获得高摩尔转化率的L-2-氨基丁酸。这一研究为生物制备L-2-氨基丁酸提供了新的方法和策略。
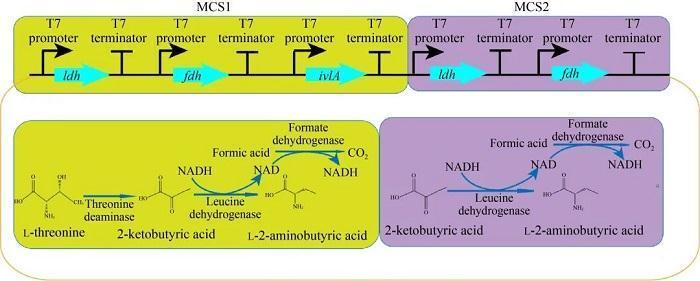
图1 多酶级联表达制备l-2-氨基丁酸的示意图
截短Loop处的氨基酸可以大幅影响酶活力,而且364–374位氨基酸的截短则显著提高了比酶活。
使用GROMACS进行分子动力学模拟,发现突变体的结构更稳定,截短后蛋白构象更紧密,底物更易结合,酶活提高。
菌株E. coli BL21/pACYCDuet-RM具有明显的优越性,摩尔转化率相较于其他菌株提高了74.6%、39%。
最适转化条件为pH7.5、温度35℃、最适底物浓度80 g/L,此时重组菌E. coli/ pACYCDuet-RM产量达到最大值66.4 g/L,产率接近100%。
通过5 L发酵罐全细胞转化制备,可以获得高摩尔转化率的L-2-氨基丁酸。
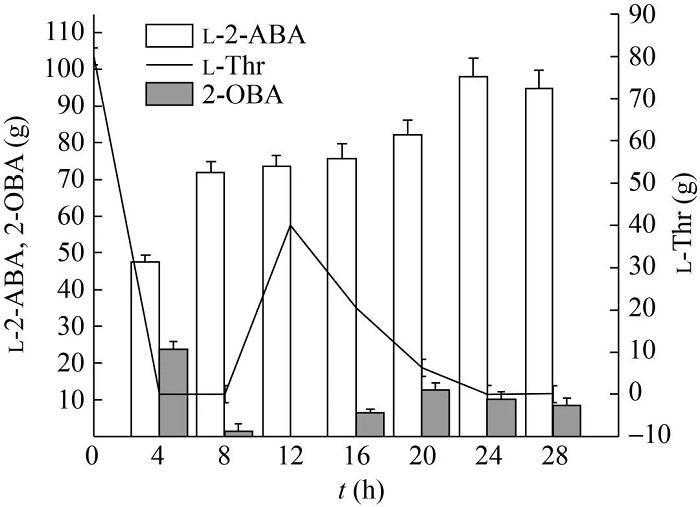
图2 5 L发酵罐全细胞转化制备l-2-ABA

