离子选择性电极是一种用于测定离子活度和指示滴定终点的工具。
1. 电池电动势和离子活度的关系
与pH玻璃电极测定溶液pH值类似,离子选择性电极通过将其插入被测溶液中与参比电极组成一个原电池,并测量其电动势来测定离子活度。例如,使用氟离子电极测定F-活度时,可以组成如下的电池:
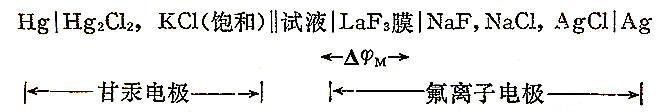
电池电动势E = (φAgCl/Ag + ΔφM) - φHg2Cl2/Hg
其中ΔφM = K - 0.059lgaF-
因此,E = φAgCl/Ag + K - φHg2Cl2/Hg - 0.059lgaF-
其中φAgCl/Ag、K、φHg2Cl2/Hg为常数,可以合并为一个常数K'
E = K' - 0.059lgaF-
对于不同的离子选择性电极,可以得到以下一般公式:
E = K' + 0.059/nlga阳离子
E = K' - 0.059/nlga阴离子
这表明在一定条件下,工作电池的电动势与被测离子活度的对数成直线关系。

2. 测定离子浓度的方法
在实际分析工作中,通常需要测定离子的浓度而不是活度。可以使用以下两种方法进行测定:
(1) 标准曲线法:配制一系列已知浓度的标准溶液,加入一定量的惰性电解质以保持各溶液离子强度一致。将离子选择性电极和参比电极插入溶液中,测量各溶液的电动势E,并根据测得的E和相应的浓度c绘制E-lgc的标准曲线。通过测量试液的电动势E,并在标准曲线上查找对应的浓度。
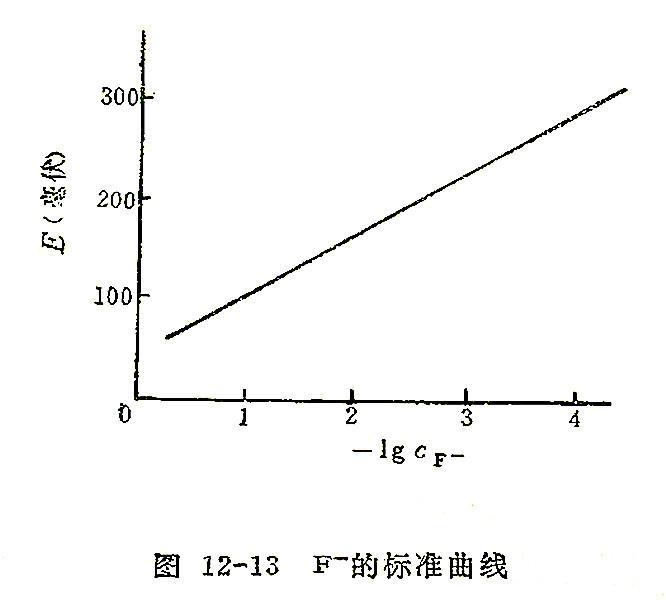
需要注意的是,离子选择性电极膜电位与离子活度呈线性关系,但只有在溶液离子强度一致时,膜电位与离子浓度才呈线性关系。因此,必须加入一定量的惰性电解质以固定溶液离子强度,从而使E与-lgc成线性关系。
(2) 标准加入法:此方法不需要知道溶液的离子强度,也不需要绘制标准曲线,只需测量二次电动势即可求出被测离子的浓度。对于复杂的试样,使用此方法非常方便有效。
方法原理是:先在试液(浓度为cx)中测得电动势为E1,然后加入浓度为cs体积为Vs的标准溶液(Vs比试液体积Vx约小100倍),再测量其电动势为E2。
E1 = K + slgrcx
E2 = K + slgr'(cx + c△)
其中r'为加入标准溶液后的溶液离子活度系数,c△为加入标准溶液后试液浓度的增量。
由于加入的体积Vs很小,不会影响溶液总离子强度,所以r=r'。因此,△E = slg(cx + c△)/cx。
通过计算△E、s和c△的值,可以得到cx的浓度。

