学生讲义之一(Student Handout I)
实验介绍
本实验採用微量化学实验,在进行氧化还原滴定之前,学生或教师事先组装简易滴定架、自製微量滴定管和自製小型电磁搅拌器(图一的左图和右图),作为氧化还原滴定的装置。以市售的优碘液中的有效碘及玉米粉所製成澱粉指示剂,进行碘直接滴定法,来测定市售的维他命C沖饮包中含抗坏血酸的毫克

图一 自製微量滴定管及滴定架(左)和自製电磁搅拌器(右)
市售维他命C沖饮包中的主要成份为抗坏血酸(L-ascorbic acid, C6H8O6),是一种还原剂,容易被氧化成去氢型的抗坏血酸(dehydro-L-ascorbic acid, C6H6O6),因此可考虑以I2为氧化剂,对维他命C进行氧化还原滴定,来测定此沖饮包中抗坏血酸的含量,其反应如反应式[1a]和[1b]所示:
I2(aq) + C6H8O6(aq) → 2I-(aq) + 2H+(aq) + C6H6O6(aq)? ? [1a]
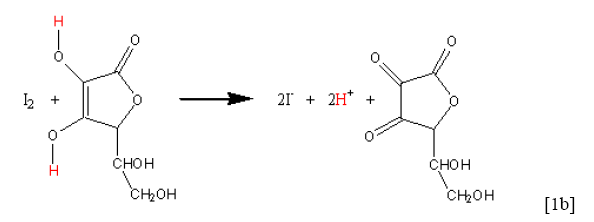
反应式来源:http://www.chem.ubc.ca/courseware/123/tutorials/exp9A/
本次实验所使用碘分子,係来自于一般药局贩售的优碘溶液(Povidone iodine Solution),此碘溶液先用硫代硫酸钠标定,然后以此优碘溶液滴定维他命C沖饮液,并添加少许的玉米粉所製成的澱粉指示剂(starch indicator)。当达滴定终点时,维他命C沖饮液中的抗坏血酸完全被碘分子氧化,而溶液中多余的碘分子便与澱粉指示剂作用,形成深蓝色错合物,如反 应式[2]所示:
I2(aq) + starch(aq) → I2-starch complex(aq)(蓝色错合物)? ? [2]
当滴定达当量点时,氧化剂(碘分子,I2)和还原剂(抗坏血酸,C6H8O6) 的当量数相等,进而计算维他命C沖饮包中抗坏血酸的毫克数。由反应式[1a]得知,1莫耳的碘分子能够与1莫耳的抗坏血酸反应。若知道每次滴定使用碘分子 的浓度及体积,则可得知碘分子的莫耳数。若再知道抗坏血酸的莫耳质量(分子量),则可得知每次滴定使用维他命C沖饮液中抗坏血酸的毫克数。若知道一次滴定 使用沖饮液的体积为整包体积的倍数,则可以计算整包含抗坏血酸的毫克数。
A. 自组简易滴定架
A1. 使用器材
1. T型压克力展示板(A4 Size)??1个/组
(例如品名:Deflect-O Classic Image Stand-Up Double-Sided Plastic Sign Holder)
2. POP夹具(中纸夹含长盘)??1个/组
3. POP夹具(中夹含吸盘)??1个/组
4. 双面胶??1个/组
A2. 组装说明
1. 自书局购得T型压克力展示板作为简易滴定架 的主体。
2. 用双面胶黏贴中纸夹(含长盘)在T型压克力展示板上方,用来夹住并固定自製微量滴定管,如图二所示。
3. 重压中夹(含吸盘),使其吸住在T型压克力展示板下方的适当位置,用来支撑注射针筒,如图二所示。

图二 简易滴定架组件及组成外观
B. 自製微量滴定管
B1. 使用器材
1. 吸量管(10 mL)??1支/组
2. 三通塑胶活栓??1个/组
3. 塑胶注射针筒(10 mL,含针头)??1支/组
4. 细砂布??1/8张/组
5. 橡皮管(6号)??约2 cm/组
6. 细铜线(直径约0.5 mm)??约10 cm/组
7. 塑胶杯(或烧杯)??1个/组
B2. 组装过程
1. 取一段长约2 cm的橡皮管两端分别连接一支10 mL的吸量管和一个三通塑胶活栓,用一小段细铜线紧密地环绕固定橡皮管与三通塑胶活栓的一端,以避免滴定液从连接的缝隙处漏出,如图三所示。

图三 微量滴定管的组装
2. 为了降低滴定的液滴大小,提高滴定的精确性,在三通塑胶活栓的下方流出管口换成一支被磨平的注射针头。为了避免在滴定过程中刺伤皮肤,此注射针头的尖端可以放置在粗砂布上以旋转方式磨平尖端。然后套入三通塑胶活栓的出口处,组装成微量滴定管,如图四所示。

图四 磨平的注射针头套入三通塑胶活栓
3. 用简易滴定管架的中纸夹夹住微量滴定管,其高度恰好使一支注射针筒能够紧密地插入三通塑胶活栓的左侧孔,形成一套微量滴定装置,如图五的左图所示。然后,旋转三通塑胶活栓成为三箭头不朝下的位置,此时滴定管呈现关闭状态,如图五的右图所示。

图五 微量滴定装置(左)及滴定管关闭状态(右)
请按此连结,参阅「学生讲义二」

