学生讲义之一(Student Handout I)
实验介绍
本实验採用简易型酸硷度计、PE滴管、10.00 mL的量筒、已标定的NaOH标準溶液及自製小型电磁搅拌器(图一的左图和右图),作为酸硷滴定的装置。并且透过两点电位法酸硷滴定,来测定食用醋中醋酸的浓度。

图一 简易型酸硷度计、PE滴管、量筒及自製小型电磁搅拌器
使用NaOH标準溶液测定食用醋中醋酸的浓度,是属于酸硷滴定中-强硷滴定弱酸-的类型,当量点pH > 7。传统上,採用酸硷指示剂判定滴定终点。本实验採用两点电位法来判定滴定终点,与指示剂法不同。两点电位法是在滴定接近当量点前,记录两组滴定体积和pH值的数据(V1,pH1 和V2,pH2 ),透过下面推导的最后式子[式9],计算出在当量点所需要的NaOH标準溶液的真正体积,并藉由化学计量计算出食用醋中乙酸的浓度。
本实验以NaOH标準溶液测定食用醋中醋酸的浓度为例,说明两点电位法在当量点时推导所需NaOH标準溶液的体积之过程。在此,假设醋酸(CH3COOH)的初浓度为C0,待测液体积为V0 ;而且假设NaOH标準溶液的初浓度为C。在当量点时,所消耗NaOH标準溶液的体积设为Ve,依酸硷中和公式,酸和硷的莫耳数相等,可得[式1]:
C0×V0 = C×Ve [式1]
在当量点前,加入NaOH标準溶液的体积设为V,此时溶液形成CH3COOH-CH3COONa的缓冲溶液。为了计算在当量点前缓冲溶液各物种的pH值,进而推导在当量点时所需要NaOH标準溶液的体积。首先,知道在当量点前缓冲溶液各物种的莫耳数。
CH3COOH? ?+? ?NaOH? ?→? ?CH3COONa? ?+? ?H2O
起始时CH3COOH莫耳数? ?? ?C0×V0
当量前使用NaOH莫耳数? ?? ?? ?? ?? ?? ?? ?? ?? ???C×V
当量前CH3COOH莫耳数 (C0×V0) – (C×V)
当量前CH3COONa莫耳数? ?? ?? ?? ?? ?? ?? ?? ?? ?? ?? ?? ?? ?? ?? ?C×V
然后,确定在当量点前缓冲溶液CH3COOH和CH3COONa的浓度,分别如[式2]和[式3]所示。


接下来,计算缓冲溶液的pH值,如下所述。先利用缓冲溶液的Henderson–Hasselbalch equation,如[式4]所示。再代入[式2]和[式3]到[式4],求得此时溶液的pH值,如[式5]所示。

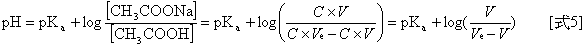 在接近当量点前,记录两组滴定体积和pH值的数据(V1,pH1 和V2,pH2 ),代入[式5]中,分别得下列[式6]及[式7]:
在接近当量点前,记录两组滴定体积和pH值的数据(V1,pH1 和V2,pH2 ),代入[式5]中,分别得下列[式6]及[式7]:
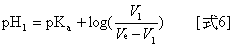
 此时[式7]减[式6],可得下列[式8]:
此时[式7]减[式6],可得下列[式8]:
 最后,整理[式8],可得在当量点时所需要NaOH标準溶液的体积(Ve),得到[式9]。
最后,整理[式8],可得在当量点时所需要NaOH标準溶液的体积(Ve),得到[式9]。
 自製小型电磁搅拌器
自製小型电磁搅拌器
A. 使用器材
1. 电脑散热风扇??1个/组
2. LM317(三端子可调整稳压IC)??1个/组
3. 220欧姆电阻??1个/组
4. 1000欧姆可变电阻??1个/组
5. 9伏特电池盒(附开关,含9V乾电池)??1套/组
6. 快乾胶??2条/班
7. 小型麵包板??1个 /组
8. 跳线??数条/组
9. 小磁铁 2枚/组
10. 扁平纸盒或塑胶盒(如1号滤纸空盒)??1个/组
11. 塑胶容器(小型)??1个/组
12. 小磁石??1个/组
B. 组装过程
1. 依照图二的线路图,布线相关电子零件于麵包板上,完成电磁搅拌器的控制电路。

图二 电磁搅拌器的控制电路
2. 以快乾胶对称黏贴两块小磁铁在电脑散热风扇的背面上。黏贴时,一块小磁铁的S极朝上与另一块N极对称朝上放置,如图三所示。

图三 黏贴两块小磁铁在电脑散热风扇的背面上
3. 在扁平纸盒或塑胶盒(如1号滤纸空盒)的一边割出一个小洞以导出电线,再黏贴散热风扇组在扁平盒内。连接散热风扇电源排线至电磁搅拌器的控制电路上,并且连接控制电路到一个9伏特电池盒(附开关,含9V乾电池),形成一个自製小型电磁搅拌器,如图四所示。

图四 自製小型电磁搅拌器
C. 操作说明
1. 放置一个小磁石到一个含有待测液的塑胶容器中,并放置于自製小型电磁搅拌器的正上方,如图五所示。

图五 待测液在塑胶容器中
2. 调整控制电路中的可变电阻,以调整适当的搅拌速率,如图六所示。

图六 调整可变电阻以控制搅拌速率
3. 準备一支PE滴管、一支10.00 mL的量筒、待测液的塑胶容器及自製小型电磁搅拌器,完成滴定实验的準备工作,如图七所示。

图七 滴定实验的装置
连结:简易的滴定终点判定-两点电位法(Two-point Potentiometric Titration)〔II〕

