血涂片在临床操作中经常使用,但你是否遇到过以下情况呢?你是否注意到它们的染色差异?A图的细胞染色非常艳丽鲜红(缓冲液pH6.4),B图的细胞染色适中(缓冲液pH6.8),C图的细胞染色呈灰蓝色(缓冲液pH7.4)。
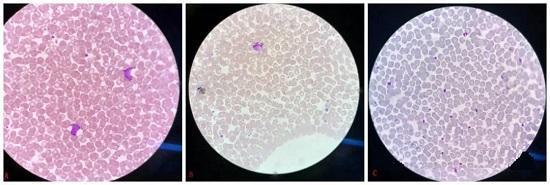
这种染色鲜艳程度的差异不仅出现在临床操作中,我们在查找不同的参考书和图谱时,细心留意也会发现这种差异。
答案就是我们使用的染色缓冲液!
瑞氏-姬姆萨染色法于1902年提出,但直到1920年Majunkin才提及缓冲液的使用。瑞氏姬姆萨复合染色使用的缓冲液是磷酸盐缓冲液。
缓冲液的两个指标会影响染色效果,一个是pH值,另一个是离子强度(摩尔浓度)。
细胞中的大部分蛋白质都是两性电解质,其带电荷会随环境的pH值改变而改变。对于某种蛋白质来说,如果缓冲液的pH<pI(蛋白质的等电点),蛋白质就会带正电荷,容易与酸性伊红结合,从而使细胞染成鲜红色。相反,如果缓冲液的pH>pI(蛋白质的等电点),蛋白质就会带负电荷,容易与美蓝天青颗粒结合,从而使细胞溶液染成灰蓝色。
为了适度染色,避免过度鲜红或灰蓝对判断的干扰,实验证明缓冲液的pH值应该在6.4~6.8之间。
离子强度(摩尔浓度)即稀释程度。1920年Majunkin提出使用缓冲液配合染色时,提出的浓度是0.057mol/L,但后来的研究发现,这种浓度的缓冲液染色时间长,容易产生染色沉渣,染色效果不理想,因此提出了低离子浓度方案(<0.033mol/L)。
高浓度的缓冲液会导致染色不良,主要是因为缓冲液中的离子与染料中的离子竞争性结合,使细胞着色变慢,需要延长染色时间。此外,这些结合后的离子更容易析出形成沉渣,影响染色效果。
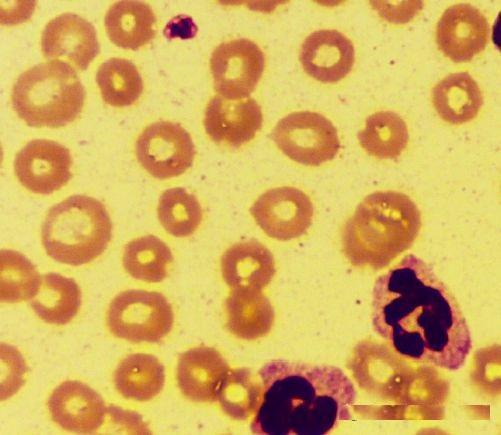
背景中有大量沉渣颗粒。
解决方案是配制适当浓度的缓冲盐溶液,并使用盐酸调整缓冲液的pH值。
例如,我们使用的这种商品化缓冲盐,按照说明书推荐的蒸馏水量加倍稀释,使用pH试纸测试pH值,并使用盐酸进行调整。
1 梁维岗,李喜萍,樊菊娥. 血细胞姬姆萨瑞氏染色法中使用缓冲液的探讨,临床检验杂志,1996.14(6):318-319
2 Majunkin, F A. JAMA, 1920.74:17

