配位错合物的化学反应
配位错合物的化学反应主要有氧化还原反应及配位基取代两大类:
1.氧化还原反应:
配位错合物中的氧化还原反应可归纳为内圈(inner sphere)及外圈(outer sphere)电子转移两种机制。内圈电子转移的机制是由1983年诺贝尔化学奖得主亨利陶比(Henry Taub)提出的,比较方程式 图一 Fe(CN)64- 与Ir(Cl)62-的氧化还原反应-外圈电子转移 一般而言,如果反应中电子转移的速率比配位基取代来得快,反应会循外圈电子转移的机制,通常发生在反应物较安定、配位基不活泼或是缺乏适合桥键配位基的情况下。 ?2.配位基取代: 配位基取代是指配位化合物中的配位基被另一配位基置换,这是由于配位基对金属离子的结合强度不同,或是活性差异所致。以 又如在粉红色含 由于加入浓盐酸可提供相较于饱和氯化钠溶液更高浓度的氯离子,依据勒沙特列原理,可使方程式 再以血红素为例,氧气、二氧化碳及一氧化碳都能与血红素形成配位错合物,但它们的结合能力并不相同,一氧化碳对血红素的亲和力是氧气的200~250倍,当动物吸入过量一氧化碳,将导致缺氧甚至可能危及性命。 ------ 参考资料: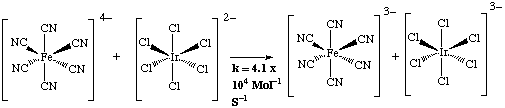
http://www.chem.ox.ac.uk/icl/dermot/mechanism1/lecture3/default.html ?为例,在
?为例,在  ?溶液中加入氨水,
?溶液中加入氨水, ?可取代
?可取代  ?形成
?形成 ![\mathrm{[Co(NH_3)_6]^{3+}}](http://highscope.ch.ntu.edu.tw/wordpress/wp-content/plugins/latex/cache/tex_8960b9c255c976ef2f22ddb3bb1c9216.gif) ,滴入硝酸银溶液后观察到生成白色氯化银沉澱,可知原先的配位基
,滴入硝酸银溶液后观察到生成白色氯化银沉澱,可知原先的配位基  ?已被置换出来,进而与银离子产生沉澱,如方程式
?已被置换出来,进而与银离子产生沉澱,如方程式  所示。
所示。![\begin{multline*}\mathrm{CoCl_{3(aq)}+6NH_{3(aq)}+3AgNO_{3(aq)}}\\ \rightarrow\mathrm{3AgCl_{(s)}+[Co(NH_3)_6]^{3+}_{(aq)}+3NO_3^{-}}\end{multline*}~~~~~~(3)](http://highscope.ch.ntu.edu.tw/wordpress/wp-content/plugins/latex/cache/tex_888e776cb979d5005d6eb3a38fc54c6f.gif)
![\mathrm{[Co(H_2O)_6]^{2+}}](http://highscope.ch.ntu.edu.tw/wordpress/wp-content/plugins/latex/cache/tex_a518600f981d6f699151f4a5e95b6290.gif) ?的水溶液中加入浓盐酸,可得到深蓝色
?的水溶液中加入浓盐酸,可得到深蓝色 ![\mathrm{[Co(Cl)_4]^{2-}}](http://highscope.ch.ntu.edu.tw/wordpress/wp-content/plugins/latex/cache/tex_c2c8151d219734f322cdb8f9078e7756.gif) 水溶液,此为可逆反应,如方程式
水溶液,此为可逆反应,如方程式  所示:
所示:![\mathrm{[Co(H_2O)_6]^{2+} + 4Cl^-\rightleftharpoons [Co(Cl)_4]^{2-}+6H_2O}~~~~~~~~~(4)](http://highscope.ch.ntu.edu.tw/wordpress/wp-content/plugins/latex/cache/tex_389fdaf87b255340c999df5c16a3d7cb.gif)
 利于向右方进行。
利于向右方进行。

