电解质可以根据其在溶液中电离的程度来区分为强电解质和弱电解质。弱电解质只有少部分电离,存在着电离平衡;而强电解质在稀溶液中几乎全部电离,没有电离平衡。然而,实际测量的电离度并不是100%,这是因为强电解质溶液中存在着离子氛,离子之间相互牵制导致离子的效能降低。为了计算离子的活度,需要引入活度系数。离子的活度、活度系数和浓度之间的关系可以表示为:
a = f · c
其中f可以因为其他电解质的加入而减小,这就是盐效应。
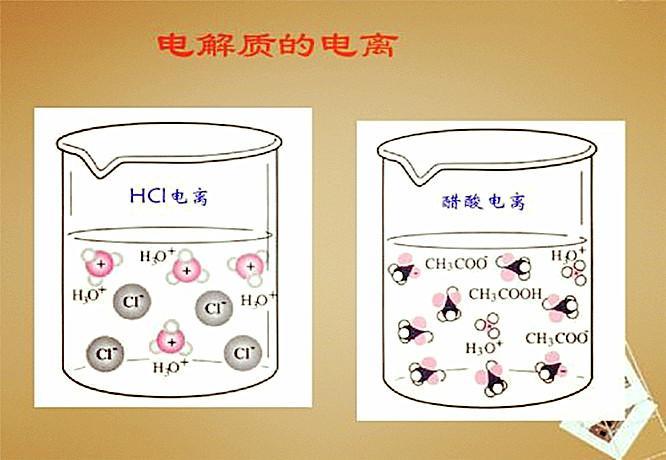
电离平衡的特性
(1)水的离子积:水是一种很弱的电解质,存在着自偶电离平衡。水的离子积常数Kw在室温(约22℃)时为1.0×10(-14次方)。纯水或稀水溶液中的〔H+〕与〔OH-〕的乘积始终等于Kw,即〔H+〕〔OH-〕=1.0×10(-14次方)。因此,可以用〔H+〕或〔OH-〕的浓度来表示溶液的酸碱性:
酸性:〔H+〕>1.0×10(-7次方)M
中性:〔H+〕=1.0×10(-7次方)M
碱性:〔H+〕<1.0×10(-7次方)M
水溶液的酸碱度还可以用pH或pOH来表示:
pH=-lg〔H+〕;pOH=-lg〔OH-〕
两者的定量关系为:pH+pOH=pKw=14
(2)电离常数:电离平衡中的平衡常数称为弱电解质的电离常数(Ki)。弱电解质的分步电离对应于每一级平衡都有一个电离常数,称为逐级电离常数。多元弱电解质的电离常数是逐级减小的。电离常数是衡量弱电解质特性的重要数据,可以用来计算电离度、离子和分子的浓度以及溶液的酸碱度。
(3)电离平衡的移动:电离平衡可以因为各种原因而发生移动。其中,同离子效应是比较重要的因素。在弱电解质溶液中,如果加入含有相同离子的强电解质,会使电离平衡向生成分子的一方移动,导致电离度大大降低。此外,溶液浓度的变化和盐效应也会对电离平衡产生影响。
(4)缓冲溶液:由弱酸和其盐或弱碱和其盐组成的溶液体系称为缓冲溶液。缓冲溶液具有抵御少量外来酸碱并维持原有pH值的能力。缓冲溶液的酸碱度可以用以下公式计算:
对弱酸和其盐体系:〔H+〕=Kac酸/c盐 或 pH=pKa-lgc酸/c盐
对弱碱和其盐体系:〔OH-〕=Kbc碱/c盐 或 pOH=pKb=lgc碱/c盐
(5)盐类水解:除了强酸强碱盐,其他盐在水溶液中都会发生水解。弱酸强碱盐的水解是阴离子水解,溶液呈碱性;强酸弱碱盐的水解是阳离子水解,溶液呈酸性;弱酸弱碱盐的水解是阳离子和阴离子同时水解,溶液的酸碱性取决于生成酸和碱的相对强度,可能是酸性、碱性或中性。盐类水解平衡的平衡常数称为水解常数,可以用来计算水解后盐溶液中各离子和分子的浓度、溶液的酸碱度以及盐的水解度。

