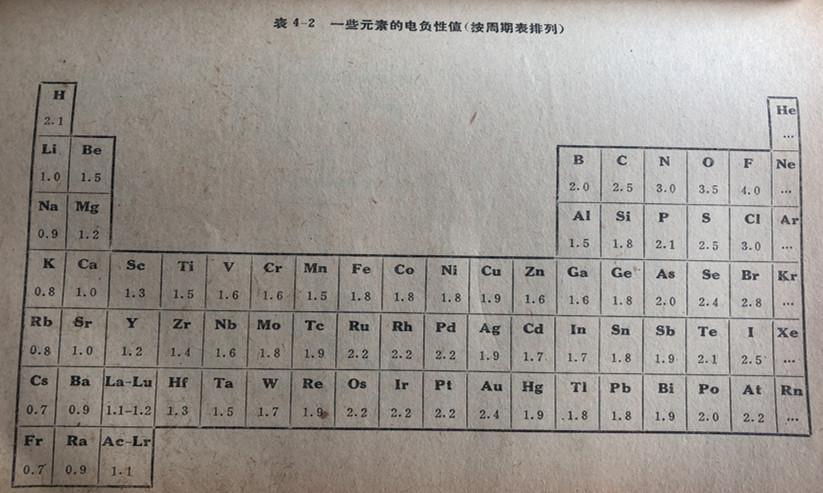
在化学中,有许多稳定的化合物,它们的分子中的所有原子并不都具有惰气结构。举例来说,硼原子有3个价电子,在稳定的BC13分子中,硼原子与3个氯原子共用了电子对。虽然原子的这种结合给每个氯原子以氩的结构,硼原子在其外电子层有6个电子而并不具有惰气的电子排布。此外,元素的原子如果外电子层是M层或更高能层,它可以同其它原子共用不止4对电子而形成共价键。举例来说,在PF。分子中的磷原子共用了5对电子,或总共10个电子,而惰气原子在它的最外层中限定最多只能有8个电子。磷原子的最外电子层(即M层)的理论最高容量是18个电子或9对电子,但从来未见有分子处于这种状况。在SFs分子中硫原子共用了6对电子(12个电子),而在IFr中碘原子共用了7对电子。在OF8中有8对共用电子。在一些情况中,最外电子层中的电子数超过了8个,但有些电子对是未被共用的。在F5和XeF4中就有这种情况。
共价化合物如BCls、PCl和IFx的形成,为惰气结构或即八隅体规则提供了一个补充原则,即在分子结构中电子倾向于成对。换句话说,我们可以说,在大多数共价分子中的原子倾向于彼此共用电子对而达成稳定的状况。因此,硼原子因其仅有3个价电子而仅能形成3个共价键,在BCl3分子中通过形成3个电子对键而取得了稳定状态。
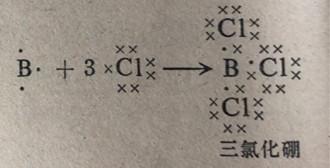 我们已经看到,在氯化氢分子中,氯原子对电子对键的电子的吸引要强于氢原子对电子的吸引,以至于电子不是均等地为2个原子所共用。一种原子对共价键中电子所表现出的吸引本能叫做电负性。电负性是一种原子对它外层电子吸引力的一种衡量尺度。许多元素的电负性值提供在表4-2中。这些数值是以一种人为选定的标度为基础的,它们的含义表明,举例来说,我们不能说氟的电负性(4.0)是硼的电负性(2.0)的两倍。表列电负性值并不是绝对电负性,但它们确可为电负性差提供了衡量尺度。举例来说,硼(2.0)和氮(3.0)之间的电负性差同氮(3.0)和氟(4.0)之间间的电负性差是相同的。
我们已经看到,在氯化氢分子中,氯原子对电子对键的电子的吸引要强于氢原子对电子的吸引,以至于电子不是均等地为2个原子所共用。一种原子对共价键中电子所表现出的吸引本能叫做电负性。电负性是一种原子对它外层电子吸引力的一种衡量尺度。许多元素的电负性值提供在表4-2中。这些数值是以一种人为选定的标度为基础的,它们的含义表明,举例来说,我们不能说氟的电负性(4.0)是硼的电负性(2.0)的两倍。表列电负性值并不是绝对电负性,但它们确可为电负性差提供了衡量尺度。举例来说,硼(2.0)和氮(3.0)之间的电负性差同氮(3.0)和氟(4.0)之间间的电负性差是相同的。
可注意到非金属元素总地来说比金属元素有较高的电负性值。氟是化学活性最强的非金属,它有最高的电负性(4.0),铯是化学活性最强的金属(钫可能是例外),它有最低的电负性(0.7),由于金属元素有相对较低的电负性并在化合物中倾向于取得正电荷,我们常说它们是电正性的,反之,非金属元素是电负性的。