螯合是一种金属离子与阴离子或分子特定的结合方式,涉及单一中心原子与多牙配位基之间形成至少两个以上的多重配位共价键。这类的配位基多半为有机化合物,称为螯合基(chelants)或螯合剂(chelating agents)。在1920年Mogan & Drew最早使用”有螯的”(chelate)这个词,衍生自龙虾或甲壳类动物的大钳,此名称暗示多牙基像螃蟹一样用两只大钳紧紧夹住猎物般箝住中心原子,如此在结构上可形成一杂环,如图一所示。
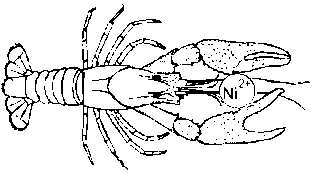
图一:螯合物(取自http://wwwchem.uwimona.edu.jm/courses/chelate.html)
螯合效应(chelate effect)
螯合效应是指针对相同的中心金属原子而言,螯合基相较于类似的非螯合基(单牙基)有更强的亲和力。以铜离子为例,在水溶液中分别与乙二胺及甲胺形成错离子,其平衡方程式如下:
Cu2+?+ en???[Cu(en)]2+??? (1)
Cu2+?+ 2 MeNH2 ???[Cu(MeNH2)2]2+??? (2)

在图二中,双牙基乙二胺与铜离子形成螯合离子,此螯合作用形成五员环。在溶液中错离子的稳定性是指在平衡状态时,配位基与中心原子结合的程度,从量化的观点来看,可由此结合的稳定性/生成平衡常数的数值大小来判断。图三中的配位基则是两个单牙基-甲胺,大约具有相近的配位能力(donor power),亦即两反应中Cu-N键的生成热大约是相同的。实验数据显示,在相同的[Cu2+],[MeNH2]为[en]的两倍下,式(1)得到的错离子浓度将会高于式(2)。前述两个方程式中,达平衡时各物种的关係表达如下:
[Cu(en)] =β11[Cu][en]
[Cu(MeNH2)2]= β12[Cu][MeNH2]2
其中β11及β12称为稳定性常数,也就是反应的平衡常数,实验结果得知[Cu(en)]高于[Cu(MeNH2)2],因此可推知β11大于β12。换言之,二牙基的乙二胺相较于两个单牙基甲胺,前者与Cu2+形成的错离子有较高的稳定性,这项在实验中观察到的现象称之为螯合效应。此效应会随着螯合环的数目而增强,因此六牙基的EDTA形成之错合物,其浓度远高于两个单牙的氮配位基以及四个单牙的羧酸根配位基所形成之错合物。
若从热力学的观点来探讨,平衡常数(K)、反应热(ΔH)、温度(T)与熵(ΔS)的关係可从自由能(ΔG)来看:
ΔG○?= ?RT ln?K?= ΔH○? TΔS○?? R:理想气体常数
前述已提过这两个形成错离子反应的生成热相近,由上式可知,两个反应其平衡常数的差异应该来自于熵的贡献。比较方程式(1)与(2),前者反应前后粒子数的改变是2→1,后者是3→1,这意味着螯合基形成错离子时,其乱度的损失是较少的,这是导致两者熵的差异其中一项因素。我们可以从另一组类似的反应来检视相关数据,如表一所示,表中的数据显示两反应的反应热确实很接近,自由能的差异主要来自熵的差异,由此可知螯合基形成的错离子,相较于结构类似的单牙基,前者在热力学上具有较高的稳定性。
表一 螯合基乙胺与单牙基甲胺形成错离子的实验数据
|
反应平衡式 |
log β |
ΔG○ |
ΔH○?(kJ/mol) |
?TΔS○(?kJ/mol) |
| Cd2+?+ 4 MeNH2???Cd(MeNH2)42+ |
6.55 |
-37.4 |
-57.3 |
19.9 |
| Cd2+?+ 2 en???Cd(en)22+ |
10.62 |
-60.67 |
-56.48 |
-4.19 |
?
参考资料:
1.螯合http://en.wikipedia.org/wiki/Chelation
2.Morgan, G. T., Drew, H. D. K. J. Chem. Soc., 1920, 117, 1456.
3.Stability, Chelation, and the Chelate Effect. http://agrss.sherman.hawaii.edu/courses/Soil640/Chelate.html

