引言:
磷酸作为一种重要的化学物质,具有多种独特的化学和物理特性,广泛应用于不同领域。
简介:
磷酸呈无色透明液体或透明结晶固体。纯固体熔点为 42.35 °C,密度为 1.834 g/cm3。液体通常为 85% 水溶液。以固体和液体形式运输。对金属和组织有腐蚀性。用于制造肥料和洗涤剂以及食品加工。
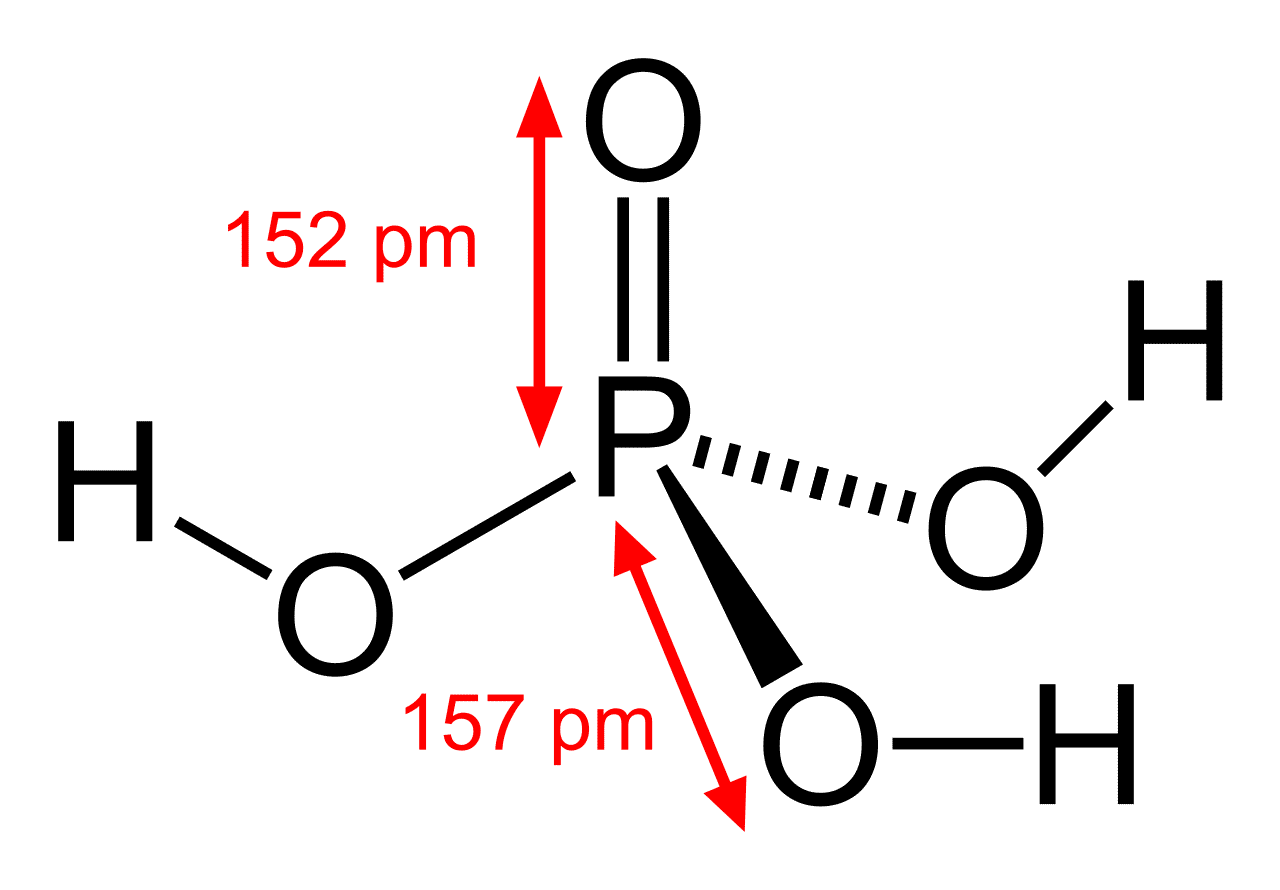
1. 磷酸的特性
1.1 磷酸的物理性质
外观:磷酸通常呈无色、无味、粘稠的液体,浓度各不相同。
状态:纯磷酸为白色结晶固体,浓缩后为无色液体。
熔点:磷酸的熔点为 42.4℃。
沸点:磷酸的沸点约为 407℃。
性质:磷酸是一种弱酸,无毒且不易挥发。
分子量:磷酸的分子量为 97.99 g/mol。
溶解度:磷酸是一种粘稠液体,易溶于水和酒精。
密度:磷酸的密度约为每立方厘米 1.6845 克(25℃ 和 85% 浓度)。
1.2 磷酸的化学性质
(1)三元酸:磷酸是一种三元酸,可以在溶液中轻松提供三个氢离子 (H+):H3PO4 + H2O ? 3H + PO4+3-
(2)热作用:加热时,磷酸可以形成二聚体、三聚体和长聚合物链,如多磷酸和偏磷酸。
(3)还原剂:磷酸可以充当还原剂,可以进行脱水反应形成不同的磷化合物。
(4)与碱的反应:当磷酸与碱反应时,会发生中和反应,从而形成三种类型的盐。磷酸与氢氧化钠的反应会形成三种盐,即 Na2HPO4、NaH2PO4 和 Na3PO4。其中一个反应方程式如下:NaOH + H3PO4 → NaH2PO4 + H2O
1.3 磷酸酸度
磷酸,也称为 H3PO4,是一种非金属磷酸盐。它是一种无机弱酸,但长时间接触会导致皮肤和眼睛受到刺激。
磷酸由三个 H 离子组成。去除三个 H 离子、两个 H 离子或一个 H 离子会分别产生磷酸根离子 (PO++++43-)、磷酸氢根离子 (HPO42-) 和磷酸二氢根离子 (H2PO4–)。
磷酸的 pH 值范围为 1.08 至 7.00(以 pH 为单位)。其 pH 值和酸度随浓度变化而变化。磷酸浓度越高,其 pH 值和酸性就越高。在低浓度下,它也可以表现为碱性。
2. 磷酸在不同行业的用途
(1)通过磷酸盐转化涂层的防锈作用
(2)作为磷-31核磁共振NMR的外部标准。
(3)在磷酸电池中。
(4)灭活碳制造。
(5)在化合物半导体处理中,选择性蚀刻铟镓砷,直至磷化铟。
(6)在微加工中选择性蚀刻氮化硅,直至二氧化硅。
(7)作为化妆品和护肤品中的pH调节剂。
(8)作为乳制品、食品和酿造产品中的消毒剂。
3. 磷酸的好处
(1)健康和营养益处
磷酸在人类健康中发挥着令人惊讶的作用。磷是磷酸的关键成分,对强健骨骼和牙齿至关重要,也有助于肌肉恢复和能量储存。虽然磷酸本身并不是我们饮食中磷的直接来源,但它在某些食物中的存在可以产生积极的影响。例如,某些饮料中的磷酸可以通过抑制细菌生长来帮助延长保质期,让我们可以更长时间地享用这些产品。
(2)农业效益
在农业领域,磷酸是提高农作物产量的宝贵工具。当用作肥料时,磷酸有助于改善土壤结构和肥力,使其成为更适合植物生长的环境。它还能提高植物养分利用的效率,确保农作物能够吸收生长所需的必需矿物质。
4. 磷酸的注意事项和副作用
磷酸不是强酸。然而,在中等浓度下,磷酸溶液会刺激皮肤。接触浓缩溶液会导致严重的皮肤灼伤和永久性眼睛损伤。处理磷酸时应穿戴适当的个人防护装备 (PPE),并应遵循适当的安全指南。
5. 有关磷酸的常见问题
(1)磷酸是什么类型的化合物?
磷酸被归类为无机弱酸。它是一种弱酸,这意味着它在溶于水时不会完全分解成离子。磷酸的化学式为 H3PO4,表明它有三个氢原子可以在反应中随时提供质子,从而赋予它酸性。
(2)磷酸的另一个名称是什么?
磷酸有时也被称为正磷酸。这个术语强调了酸中磷酸分子的特定结构。磷酸的 IUPAC 名称是 Ortho Phosphoric Acid。
(3)磷酸的密度是多少?
磷酸的密度会根据其浓度而变化。浓缩磷酸的浓度通常约为 85%,密度约为 1.69 g/mL。但是,确切的密度将取决于磷酸溶液的具体浓度。
(4)磷酸的pH值是多少?
磷酸的pH值随水溶液浓度的变化而变化。在0.1M水溶液中其pH值为1.62,0.01M磷酸溶液的pH值为2.25。其pH值范围为1.08-7。
6. 结论
总体来看,磷酸具有多样化的物理和化学性质,这使得它在各种应用中都有重要作用。磷酸的多功能性质使其在现代化学和生物学的研究和应用中不可或缺。深入了解磷酸的特性不仅有助于优化其应用,还能推动相关领域的科学进展和技术创新。
参考:
[1]https://en.wikipedia.org/wiki/Phosphoric_acid
[2]https://www.geeksforgeeks.org/
[3]https://www.vedantu.com/
[4]https://www.palvifze.com/Blog/detail/phosphoric-acid-properties-uses-and-safety-precautions
[5]https://pubchem.ncbi.nlm.nih.gov/compound/1004
[6]https://drs.illinois.edu/Page/SafetyLibrary/MineralAcids

